Borelioza (choroba z Lyme, krętkowica kleszczowa, łac. borreliosis, ang. Lyme disease, Lyme borreliosis) – wieloukładowa choroba zakaźna wywoływana przez bakterie należące do krętków: Borrelia burgdorferi, Borrelia garinii, Borrelia afzelii, Borrelia japonica, przenoszona na człowieka i niektóre inne zwierzęta przez kleszcze z rodzaju Ixodes. Borelioza jest najczęstszą chorobą odkleszczową. Zakażenie człowieka następuje poprzez ślinę lub wymiociny kleszcza. Rezerwuarem krętka są liczne gatunki zwierząt, głównie gryzonie. Wczesne objawy choroby obejmują powstanie charakterystycznego rumienia cechującego się obwodowym szerzeniem się i centralnym ustępowaniem. Rumień wędrujący jest najczęstszym objawem wczesnej postaci boreliozy. Inne wczesne zmiany to rzadko występujący naciek limfocytarny skóry oraz objawy grypopodobne obejmujące gorączkę, ból głowy, osłabienie. Wczesne objawy ustępują w ciągu 3 miesięcy i u części chorych rozwija się postać wczesna rozsiana, która może przebiegać pod postacią zapalenia stawów lub neuroboreliozy albo (rzadziej) zapalenia mięśnia sercowego. Po wielu latach od zakażenia u części chorych dochodzi do zanikowego zapalenia skóry, przewlekłego zapalenia stawów, powikłań neurologicznych. Borelioza jest rozpoznawana na podstawie dodatnich testów serologicznych oraz występowaniem typowych objawów klinicznych. Zakażenie jest skutecznie leczone za pomocą antybiotyków z grupy penicylin, cefalosporyn oraz tetracyklin.
Historia
W 1909 roku szwedzki dermatolog Arvid Afzelius jako pierwszy powiązał rumień wędrujący z ukąszeniem przez kleszcza. W 1922 neuroboreliozę opisało niezależnie dwóch francuskich neurologów – Charles Garin i Antoine Bujadoux, a ukąszenia kleszczy z objawami neurologicznymi połączył Alfred Bannwarth w latach 40. Bannwarth, niemiecki neurolog, opisał zespół zaczynający się pojawieniem rumienia skórnego, określanego jako ECM – erythema chronicum migrans, do którego sukcesywnie dołączały objawy limfocytarnego zapalenia opon mózgowych, bóle korzonkowe i objawy zapalenia nerwów czaszkowych i obwodowych. Zespół Bannwartha obecnie jest klasyfikowany jako neuroborelioza. W 1977 roku opublikowano opis 12 przypadków zapalenia stawów u dzieci z okolic miasteczek Lyme oraz Old Lyme w stanie Connecticut i zasugerowano ich związek ze zmianami skórnymi po ukąszeniach kleszczy. Od tej miejscowości wzięła się angielska nazwa choroby, Lyme disease, która jest po angielsku również znana jako borreliosis, po polsku borelioza, od nazwiska francuskiego biologa Amédée Borrela, na którego cześć nazwano również rodzaj bakterii Borrelia. Amerykański naukowiec Willy Burgdorfer w 1983 roku wyizolował z kleszcza Ixodes dammini krętki, które później w uznaniu zasług Burgdorfera nazwano Borrelia burgdorferi. Rok później wykryto swoiste przeciwciała w klasie IgM i IgG przeciwko Borrelia burgdorferi.
Borelioza w Europie jest wywoływana przez krętki Borrelia garinii, Borrelia afzelii rzadziej przez Borrelia burgdorferi, która dominuje w Ameryce Północnej. Rezerwuarem zarazków jest około 300 różnych gatunków ssaków (głównie gryzonie z rodziny nornikowatych i myszowatych; a także wolno żyjące jelenie, sarny i wilki) oraz niektóre gatunki ptaków. Tylko niektóre zwierzęta pełnią równocześnie rolę żywicieli kleszcza i rezerwuaru krętków. Bakterie są przenoszone głównie ze śliną kleszczy z rodzaju Ixodes (w Polsce I. ricinus). Kleszcz zakaża się krętkiem poprzez żywienie się krwią zakażonych zwierząt. Kolejne stadia rozwojowe kleszcza zakażają swoich kolejnych żywicieli, powodując utrzymywanie się rezerwuaru zarazków w środowisku. 90% procent udokumentowanych przypadków boreliozy u ludzi nastąpiło w wyniku kontaktu z nimfami kleszczy. Częstość występowania zakażonych kleszczy w różnych częściach Europy waha się od 3% do 34%. W niektórych lesistych obszarach północno-wschodniej Polski odsetek ten sięga 25%.
Epidemiologia
Borelioza jest najczęstszą chorobą odkleszczową. Najwięcej zachorowań na boreliozę notuje się w północno-wschodnich stanach USA, w Europie Środkowej, Skandynawii i Rosji. Są to obszary endemicznego występowania choroby związane z obszarem bytowania kleszczy Ixodes. Nie ma pewnych dowodów na występowanie w Australii B. burgdorferi ani jakichkolwiek innych krętków przenoszonych przez kleszcze, które mogłyby wywoływać lokalne postacie boreliozy.
Polska
Większość nowych przypadków boreliozy jest notowana między 1 maja a 30 listopada, a 80% przypadków występuje w czerwcu i lipcu w okresie żerowania mikroskopijnych, trudnych do zauważenia nimf kleszczy. W Polsce rejonem endemicznym jest północna część kraju (szczególnie województwo podlaskie, warmińsko-mazurskie, zachodniopomorskie). W ostatnich latach szczególny wzrost zachorowań odnotowano w województwie śląskim i małopolskim. W 2004 roku w Polsce liczba zachorowań wynosiła 3817 (zapadalność ok. 10/100000), a w 2010 roku – 8628 przypadków.
Europa
Borelioza w Europie jest wywoływana przez krętki Borrelia garinii, Borrelia afzelii rzadziej przez Borrelia burgdorferi, która dominuje w Ameryce Północnej i jest przenoszona przez kleszcze Ixodes ricinus. Borelioza występuje w prawie każdym kraju Europy. Najwięcej przypadków zachorowań występuje w Europie Środkowej, a znacznie rzadziej w Europie Południowej.
Patomechanizm
Borrelia dostaje się do organizmu w wyniku ukłucia kleszcza. Ślina kleszcza zawiera składniki, które zakłócają reakcję odpornościową w miejscu ukłucia, co znacznie ułatwia infekcję. Odpowiedź zapalna na bakterie powoduje powstanie wczesnej zmiany skórnej (rumień wędrujący). Borrelia żyje wewnątrzkomórkowo oraz przekracza barierę krew-mózg, co stwarza pewne problemy w czasie leczenia (tylko niektóre antybiotyki penetrują barierę krew-mózg i tylko niektóre działają wewnątrzkomórkowo). W ciągu kilku tygodni po ukłuciu kleszcza krętki rozprzestrzeniają się za pośrednictwem krwi do odległych miejsc – stawów, serca, układu nerwowego. Nieleczona infekcja może być obecna przez wiele miesięcy lub nawet lat, mimo wytwarzania przeciwciał przeciw borrelii. Krętki unikają odpowiedzi immunologicznej poprzez zmniejszanie ekspresji białek powierzchniowych (które są celem układu odpornościowego), zmienność antygenową powierzchniowego białka VlsE oraz inaktywację dopełniacza.
Borrelia zwykle usadawia się w tkance łącznej (skóra, ścięgna, ściany naczyń krwionośnych, w tym w naczyniach mózgowych), w mięśniach i w tkance nerwowej (w komórkach glejowych i nerwowych). Borrelia jest znajdowana w większych ilościach we wzgórzu, korzeniach grzbietowych rdzenia kręgowego.
Uszkodzenie ośrodkowego układu nerwowego prawdopodobnie jest wynikiem przylegania krętków do komórek glejowych. Bakterie mogą indukować proliferację, a następnie apoptozę astrocytów. Krętki mogą indukować wydzielanie do komórek nerwowych pewnych substancji, w tym cytokin IL-6 i TNF-αoraz kwasu chinolinowego, które w nadmiarze stają się szkodliwe dla neuronów. Zmiany w układzie nerwowym powodowane przez boreliozę są na tyle charakterystyczne, że przez wiele lat występowały jako samodzielna jednostka chorobowa zwana zespołem Bannwartha. Istnieje hipoteza, że bakteria wytwarza toksynę bakteryjną odpowiedzialną za co najmniej część objawów choroby, takich jak zaburzenia pamięci, bezsenność oraz drętwienia kończyn i języka, oraz zaobserwowaną w tej chorobie reakcję Jarischa-Herxheimera. Wprawdzie nie istnieje test wykrywający toksyny bakterii, ale pomimo to odkryto hemolityczną aktywność Borrelia burgdorferi, a w DNA borrelii odkryto fragment kodujący odmianę jadu kiełbasianego. Wiadomo również, że ściana komórkowa bakterii zawiera toksyczny lipopolisacharyd oraz peptydoglikan mający własności prozapalne.
W patogenezie postaci stawowej największą rolę odgrywają proces rozpoznawania białka OspA (białko powierzchniowe A, wiąże krętka z białkami obecnymi w jelicie kleszcza) przez makrofagi. Dochodzi do syntezy cytokin prozapalnych i tworzenia nacieków zapalnych zawierających pobudzone komórki jednojądrzaste i fibroblasty. Odczyn zapalny powoduje proliferację błony maziowej, odkładanie się tkanki łącznej i w konsekwencji uszkodzenie stawu
Objawy kliniczne i przebieg
W ciągu od 1 do 3 tygodni od ukłucia pojawia się pojedynczy rumień wędrujący, który jest pierwszym objawem choroby. Charakterystyczne jest jego obwodowe szerzenie się i centralne ustępowanie. Rumieniowi mogą towarzyszyć objawy grypopodobne. Rzadkim objawem jest ciemnoczerwony naciek limfocytarny najczęściej na małżowinie usznej. Zarówno rumień, jak i objawy ogólnoustrojowe ustępują w ciągu 4–12 tygodni. U części chorych objawy zakażenia ograniczonego mogą nie występować lub pozostać niezauważone przez chorego. Wówczas w ciągu od kilku tygodni do kilku miesięcy choroba ujawnia się w postaci zakażenia uogólnionego (stadium wczesne rozsiane). Może przebiegać pod postacią zapalenia stawów lub neuroboreliozy albo (rzadziej) zapalenia mięśnia sercowego. Zapalenie stawów rozwija się u około 60% nieleczonych pacjentów. Znacznie rzadziej rozwija się neuroborelioza, występuje u około 15% nieleczonych. Najczęstszym powikłaniem neurologicznym jest porażenie nerwu twarzowego. Powikłania kardiologiczne są jeszcze rzadsze, dotyczą około 5% nieleczonych osób. Rzadkie jest występowanie różnych postaci klinicznych u tego samego chorego. Po wielu latach od zakażenia u pacjentów nieleczonych mogą rozwinąć się późne objawy boreliozy, które mogą doprowadzić do trwałego uszkodzenia układu nerwowego lub narządów ruchu.
Nieleczona borelioza przebiega u człowieka w trzech etapach:
- Etap infekcji zlokalizowanej:
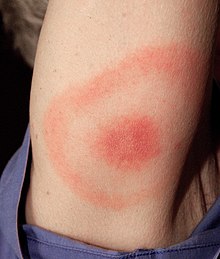
- Rumień wędrujący (rumień pełzający, erythema migrans) – jest najczęstszym objawem boreliozy. W ciągu 1–3 tygodni od ukłucia kleszcza w miejscu ukąszenia pojawia się pojedyncza rumieniowa plama lub grudka na skórze, która szybko ulega powiększeniu z centralnym przejaśnieniem. Nie występuje we wszystkich przypadkach choroby (jest nieobecna do 20% zakażeń). Rumień najczęściej jest zlokalizowany na skórze kończyn dolnych i tułowia, co jest związane z lokalizacją ukłucia. Zmiany pojawiające się w ciągu 3 dni od ukłucia należy traktować jako odczyn hiperergiczny (odczyn zwykle >5 cm, bez przejaśnienia w centralnej części). Mogą występować wtórne zmiany satelitarne. W nietypowym przebiegu zmianie może towarzyszyć powiększenie lokalnych węzłów chłonnych.
- Naciek limfocytarny (chłoniak limfocytowy skóry, limfocytoma, borrelia lymphocytoma) – przebiega jako niebolesny czerwony guzek, najczęściej na małżowinie usznej, mosznie, brodawkach sutkowych). Zmiana nieleczona może się utrzymywać nawet kilka lat. Występuje u mniej niż 1% chorych. Odpowiedzialność za wystąpienie nacieku przypisuje się gatunkowi Borrelia afzelii.
- Objawy grypopodobne.
- Rumień wędrujący, naciek limfocytarny oraz zanikowe zapalenie skóry (acrodermatitis chronica atrophicans) są patognomoniczne, to znaczy wystarczające do rozpoznania choroby.
- Etap infekcji rozproszonej:
- Nawracające zapalenie stawów – ujawnia się od 2 tygodni do 2 lat od wystąpienia pierwszych objawów boreliozy. Przebiega pod postacią nawracających kilkutygodniowych epizodów bólu i obrzęku stawów. Zapalenie zwykle dotyczy jednego lub rzadziej dwóch stawów i obejmuje duże stawy: kolanowe (najczęściej), łokciowe, skokowe, rzadziej inne. Przebieg asymetryczny. Każde kolejne zaostrzenie jest coraz łagodniejsze aż do ustąpienia dolegliwości. U niektórych pacjentów przechodzi w stan przewlekły.
- Objawy podrażnienia lub limfocytarne zapalenia opon mózgowo-rdzeniowych i nerwów obwodowych. Zapalenie opon mózgowo-rdzeniowych ma przebieg łagodny, jedynym objawem choroby może być ból głowy.
- Zapalenie nerwów czaszkowych – w stadium wczesnym najczęściej porażenie nerwu twarzowego, czasem dwustronne, może mieć nawracający przebieg.
- Zapalenie mięśnia sercowego. Stosunkowo rzadkie. Ujawnia się w postaci zaburzeń przewodnictwa jako blok przedsionkowo-komorowy o różnym stopniu. Przebiega bezobjawowo.
- Etap infekcji przewlekłej:
- Zanikowe zapalenie skóry – ujawnia się wiele lat po zakażeniu, najczęściej występuje na kończynach dolnych u osób w podeszłym wieku. Jest najczęstszym powikłaniem późnym boreliozy. Zmiany początkowo mają charakter zapalny o zabarwieniu sinoczerwonym, niesymetrycznie rozmieszczone. Mogą występować ogniska wzmożonej pigmentacji i oraz teleangiektazje. Z czasem dochodzi do zmian zanikowych ze ścieńczeniem skóry z widocznym poszerzeniem żył. Zmianom często towarzyszą parestezje i ból stawów.
- Neuroborelioza – występuje u 10-15% nieleczonych pacjentów:
- polineuropatia obwodowa – występują zaburzenia czucia i porażenia nerwów obwodowych,
- zapalenie korzeni nerwowych i nerwów obwodowych,
- zaburzenia funkcji poznawczych i pamięci.
- Przewlekłe zapalenie stawów, rzadko trwałe uszkodzenie.
- Łagodne zapalenie mięśni, ścięgien, kaletek maziowych.
Rozpoznanie
Podstawową rolę w diagnostyce boreliozy odgrywa diagnostyka serologiczna. Obecnie zalecana jest diagnostyka dwustopniowa. Pierwszy etap obejmuje badania z zastosowaniem testu serologicznego o wysokiej (nawet do 100% czułości: ELISA, test immunofluorescencyjny (IIFT), technika jakościowa ELFA. W przypadku wyniku dodatniego lub wątpliwego konieczne jest zastosowanie testu potwierdzenia – western blot, który charakteryzuje się wysoką (do 100%) swoistością.
Za pomocą testów ELISA wykrywa się przeciwciała w klasie IgM i IgG. Swoiste IgM pojawiają się we krwi po 3–4 tygodniach od zakażenia (mogą być wykrywane w drugim tygodniu choroby, ale u większości pacjentów pojawiają się później) i zanikają w ciągu 4–6 miesięcy. Swoiste IgG są wykrywalne po 6–8 tygodniach od zakażenia i utrzymują się wiele lat nawet u pacjentów skutecznie leczonych antybiotykami. Dodatni wynik badania serologicznego bez objawów klinicznych typowych dla boreliozy nie ma znaczenia diagnostycznego U pacjentów z obecnym rumieniem wędrującym rozpoznanie należy opierać na rozpoznaniu klinicznym bez potwierdzenia badaniami serologicznymi, których wyniki w tej fazie choroby często są negatywne.
Możliwe są reakcje krzyżowe na antygeny innych patogenów: wirusa Epsteina-Barr, cytomegalowirusaczy wirusa opryszczki pospolitej.
W neuroboreliozie OUN konieczne jest badanie płynu mózgowo-rdzeniowego gdzie wykrywa się przeciwciała w klasach IgM i IgG. Dla wykazania neuroboreliozy OUN istotne jest wykazanie wysokiego wskaźnika przeciwciał (stosunek zawartości swoistych przeciwciał w płynie mózgowo-rdzeniowym do zawartości w surowicy), zwykle >2.
Potwierdzenie rozpoznania zapalenia mięśnia sercowego o tej etiologii wymaga wykazania obecności przeciwciał IgM w surowicy oraz zaburzeń czynności serca potwierdzonych w EKG.
PCR jest metodą diagnostyczną pozwalającą wykryć DNA bakterii. Metoda wykazuje największą przydatność we wczesnym zakażeniu, kiedy jeszcze nie zostały wytworzone przeciwciała przeciwko krętkom Borrelia. W późniejszym etapie po wytworzeniu przeciwciał PCR jest metodą uzupełniającą, w sytuacjach gdy diagnostyka oparta o przeciwciała jest utrudniona z powodu defektów immunologicznych lub poważnych schorzeń współistniejących. PCR nie jest szeroko stosowany ze względów ekonomicznych oraz częstych wyników fałszywie dodatnich i fałszywie ujemnych Wykrycie DNA krętka nie jest jednoznaczne z aktywnym zakażeniem. Ponadto dodatni wynik nie pozwala stwierdzić, czy DNA krętkowe pochodzi z żywych czy martwych organizmów. Negatywny wynik nie pozwala ostatecznie wykluczyć infekcję.
Leczenie
Boreliozę leczy się za pomocą antybiotyków. Wybór leku zależy od postaci (etapu) choroby. W leczeniu znajdują zastosowanie: penicyliny, cefalosporyny oraz tetracykliny. Czas trwania leczenia również zależy od postaci choroby – waha się od 21 do 28 dni do 1 roku .